-
医院简介
医院介绍

类型:公立 综合医院等级:三级甲等医保:医保定点医院医院电话:010-85231777(公众与健康服务热线)预约挂号电话:010-114(24小时) 在线挂号医院网址:http://www.bjcyh.com.cn东大桥院区地址:北京市朝阳区工人体育场南路8号 查看地图乘车路线石景山院区地址:北京市石景山区京原路5号 查看地图乘车路线常营院区地址:北京市朝阳区东十里堡路3号院 查看地图乘车路线一、医院概况首都医科大学附属北京朝阳医院建于1958年,是北京市政府举办的集医疗、教学、科研、预防于一体的三级甲等综合医院;是首都医科大学第三临床医学院,北京市呼吸疾病研究所所在医院,也是北京市基本医疗保险A类定点医疗机构。医院现为一院三址,东大桥院区、石景山院区和常营院区三个院区。其中,东大桥院区和石景山院区总占地面积10.28万平米、建筑面积21万平米;常营院区占地面积7.22万… 详细>>
-
新闻中心
-
党建工作
- 科学研究
-
医学教育
您所在的位置:
首页
>>
科学研究
陶勇团队在Nature子刊发表研究成果“基于自愈合大孔微球的外泌体眼内缓释剂型”
近日,首都医科大学附属北京朝阳医院(以下简称朝阳医院)眼科主任陶勇教授基于多年的慢性眼底疾病临床诊疗经验,与中国科学院过程工程研究所生化工程国家重点实验室马光辉院士和魏炜研究员团队合作,提出了“类细胞”剂型的新策略,进行了玻璃体视网膜疾病治疗的研究,相关工作发表于Nature Biomedical Engineering上。
近年来,细胞疗法在眼科疾病治疗领域获得了越来越多的关注,并且已经在临床试验中显示出独特的疗效。然而,该创新疗法仍面临着体内细胞存活率低、病理环境下细胞表型不稳定、细胞产品保存条件苛刻等一系列难题。已有研究表明,旁分泌是细胞发挥治疗作用的机制之一。因此,科研人员开始思考利用更为稳定的细胞分泌成分(如外泌体)作为药效组分,对眼部相关疾病进行治疗。
首先,研究人员基于独创的自愈合大孔微球(Cap)来负载外泌体(Exo)。由此所构建的ExoCap体系可以在尺寸、内部结构和分泌行为方面实现对功能性细胞的模拟。此外,ExoCap在玻璃体腔中向下沉降,可以避免出现活细胞注射后漂浮在玻璃体腔中影响视野的副作用;随后,ExoCap缓慢降解,长效释放其内装载的活性外泌体。
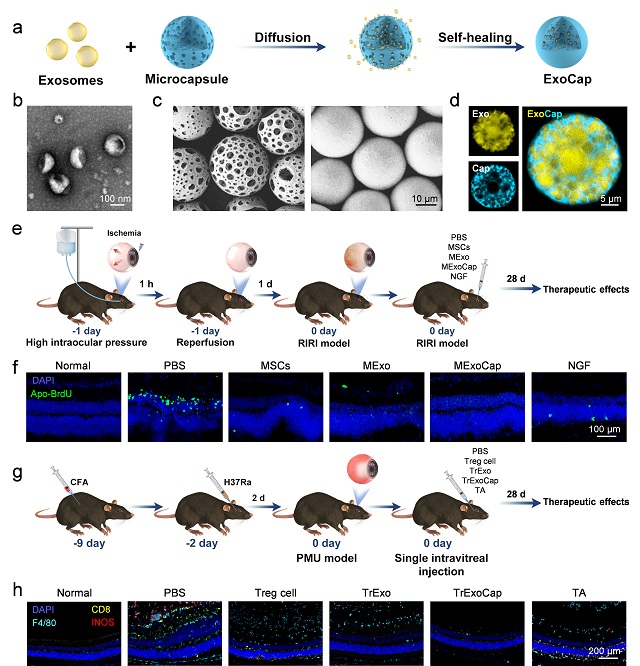
鉴于该体系构建的通用性和灵活性,可以按照不同治疗需求负载不同细胞来源的外泌体。研究人员在小鼠视网膜缺血再灌注损伤(RIRI)模型中证明,大孔微球装载间充质干细胞外泌体(MExo)可以有效地阻止视网膜细胞凋亡,效果显著优于神经生长因子(NGF)治疗方案;同时也在小鼠和食蟹猴致敏分枝杆菌性葡萄膜炎(PMU)模型中证明了,大孔微球装载调节性T细胞外泌体(TrExo)可以抑制眼内炎症,副作用较糖皮质激素例如曲安奈德(TA)治疗方案显著更低。
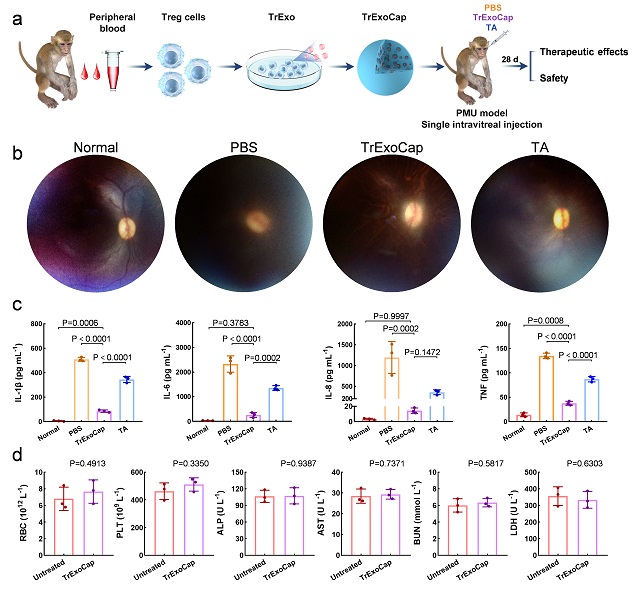
据研究人员介绍,上述成果仍属于动物水平的临床前研究,实际临床疗效仍有待进一步研究。鉴于ExoCap仅包含细胞外泌体组分和FDA批准的PLGA材料,并且在小鼠和食蟹猴模型中显示了较好的安全性和有效性,该创新剂型具有较大的临床转化潜力。研究团队正在按照相关要求合作推进临床个体化治疗的研究。
本工作是陶勇团队基于以往的研究基础,在眼底病治疗领域的新突破。包晗硕士及田颖博士为该论文共同第一作者,陶勇教授(朝阳医院)、魏炜研究员(过程工程研究所)和马光辉院士(过程工程研究所)为共同通讯作者。该工作得到了国家自然科学基金项目、北京自然科学基金项目、北京顺义区科技成果转化协调服务平台建设基金、北京市医院管理中心“登峰”人才培养计划的支持。
上一篇: 朝阳医院和北京工业大学举办项目对接活动

 京公网安备11010502033042
京公网安备11010502033042